九价HPV疫苗半年批签发930万支,约满足300万女性接种需求。
从16-26岁扩宽接种年龄至9-45岁,默沙东九价HPV疫苗适应症扩展引起广泛关注。8月30日晚间,默沙东宣布,其九价人乳头瘤病毒疫苗(酿酒酵母)(以下简称九价HPV疫苗)新适应症已经获得我国国家药品监督管理局批准,此次获批标志着默沙东九价HPV疫苗的适用人群扩展至9-45岁适龄女性。
宫颈癌是全球女性第二大肿瘤疾病,也是我国女性第二大肿瘤疾病。在市场上,世界500强之一企业默沙东的四价宫颈癌疫苗和九价宫颈癌疫苗,以及GSK的二价宫颈癌疫苗长期以来垄断全球宫颈癌疫苗市场。
目前,我国国产HPV疫苗中,有万泰生物旗下的二价HPV疫苗、沃森生物旗下公司玉溪泽润自主研发和生产的双价人乳头瘤病毒疫苗(HPV2疫苗)获得国家药品监督管理局的上市批准。
在国内市场,不同价次的HPV疫苗的供需状况也不同。九价HPV疫苗长期处于“一苗难求”局面。数据显示,上半年进入我国大陆的HPV九价疫苗为929.9万支。九价HPV疫苗采用三剂免疫程序,以此计算,约能提供给300万名女性的疫苗接种。
九价HPV疫苗扩龄,疫苗紧缺问题仍待解
全球首款HPV疫苗于2006年获批上市。目前,我国在售的进口HPV疫苗包括GSK的二价HPV疫苗、默沙东的四价HPV疫苗和九价HPV疫苗。2019年12月,万泰生物旗下二价HPV疫苗,作为国内首个二价HPV疫苗获批上市,2022年5月上海泽润的二价HPV疫苗上市。
二价、四价、九价HPV疫苗均可预防HPV16和18型感染(引发宫颈癌的两种主要HPV型别,合计共引发约70%的宫颈癌),四价HPV疫苗还可预防HPV6和11型感染(二者合计引发约90%的生殖器疣),九价HPV疫苗相比四价HPV疫苗,还可为另外5种高危型HPV感染提供保护(该5种高危型HPV合计引发约20%的宫颈癌)。
在国内市场,不同价次的HPV疫苗的供需状况也不同。九价HPV疫苗长期处于“一苗难求”局面。
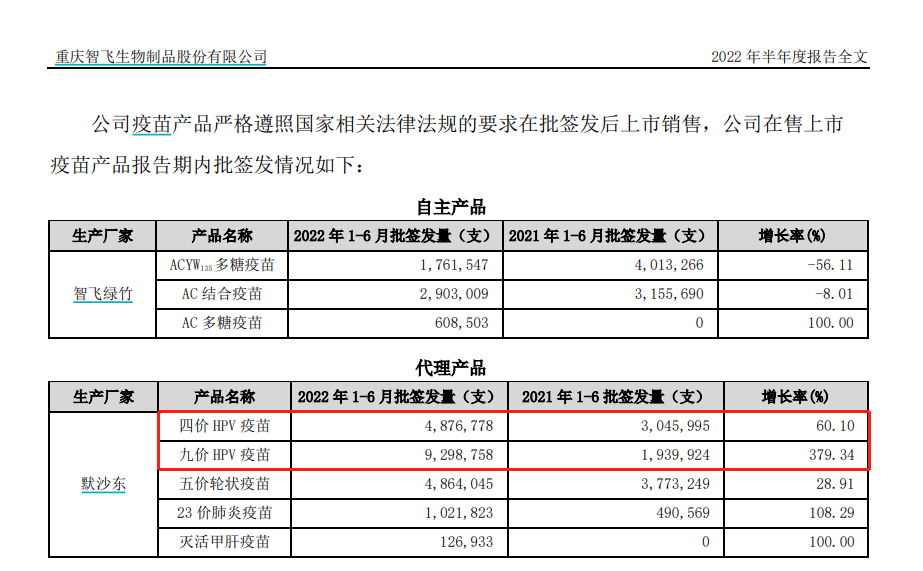
在全球HPV疫苗市场中,四价和九价HPV疫苗目前由默沙东掌握着全球最核心的生产能力以及定价权。2012年,智飞生物签下默沙东的独家代理协议,默沙东在中国大陆区向智飞生物独家供应HPV疫苗。
数据显示,上半年智飞生物所代理的默沙东四价、九价疫苗,批签发量分别为487.67万支、929.87万支。
目前,九价HPV疫苗采用三剂免疫程序。以此来看,上半年在中国大陆批签发的929.9万支疫苗,约能提供给300万名女性的疫苗接种。
此前国信证券发布研报认为,国内9-45岁适龄女性约3.6亿人,从2017年国内引进HPV产品至今,批签发总量约6500万支,折合约2000万人份,整体人群渗透率约5.5%,仍处于低位。
这意味着,HPV九价疫苗扩龄背后,九价疫苗“一针难求”局面依然有待缓解。
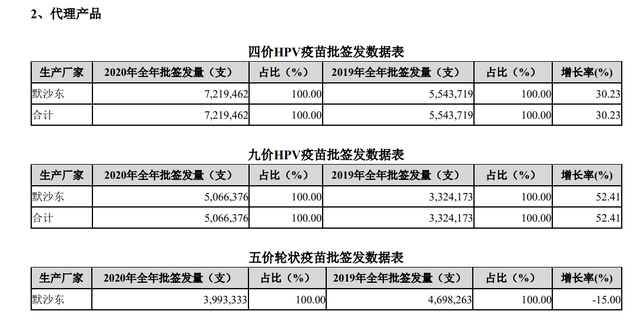
不过,国内进口的九价疫苗数量持续增加。数据显示,2020年度默沙东的四价HPV疫苗获得批签发量为721.94万支;九价HPV疫苗获得的批签发量506.6万支。
多款国产HPV九价疫苗进入临床III期,谁会成为中国“默沙东”?
在国际HPV疫苗赛道,虽然默沙东和GSK长期垄断全球宫颈癌疫苗市场,国内已经有两款二价HPV疫苗上市,且多家疫苗企业亦在争分夺秒进行HPV九价疫苗的研发、临床试验。
贝壳财经记者了解到,据了解,沃森生物(上海泽润)、万泰生物(北京万泰生物)、上海博唯、康乐卫士、瑞科生物的HPV九价疫苗均已进入临床三期阶段。
8月26日,上市公司万泰生物发布半年度报告中提到,“九价HPV疫苗III期临床试验和产业化放大进展顺利”,公司的九价HPV疫苗与佳达修9的头对头临床试验已完成临床试验现场及标本检测工作,正在进行数据统计分析,小年龄桥接临床试验完成入组工作。
万泰生物称,为了加快九价HPV疫苗的商业化进程,已经完成生产车间安装调试,顺利进入工艺转移阶段,为后续工艺验证及申报生产夯实基础。
此外,万泰生物的九价宫颈癌疫苗二期扩产建设项目、九价宫颈癌疫苗基地建设(一期)项目均在按计划进展中。
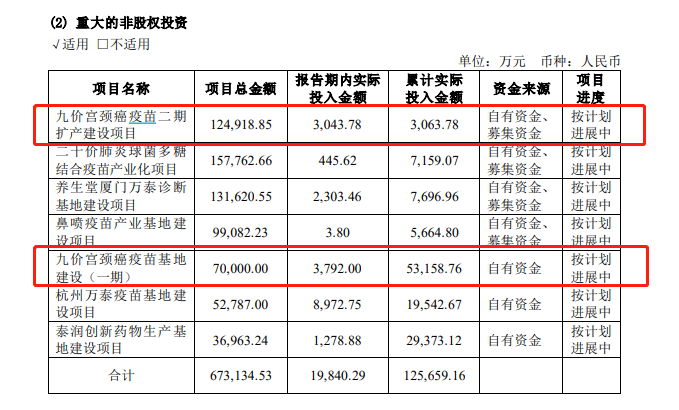
根据万泰生物半年报,截至今年6月底,九价宫颈癌疫苗基地建设(一期)项目累计实际投入金额5.3亿元,九价宫颈癌疫苗二期扩产建设项目累计实际投入金额3043.78亿元。
8月9日,上市公司瑞科生物发布公告披露HPV九价疫苗的临床试验进展称,本公司已于近日完成其重组九价HPV疫苗REC603的小年龄组免疫桥接及与Gardasil?9免疫原性比较两项研究的全部受试者入组和首剂接种工作。同时,REC603主效力试验的受试者正在按照临床方案开展随访工作。
瑞科生物表示,已完成的I期临床数据显示,REC603安全且耐受,具有良好的免疫原性。REC603采用汉逊酵母表达系统,实现了HPV病毒样颗粒的高产及稳定表达,使本公司的候选疫苗更适合做商业化生产。凭借明确的关键工艺参数及控制策略,REC603易于扩展生产规模,以满足国内及全球市场的需求。
根据上市公司沃森生物最新在8月11日披露的半年度报告,子公司上海泽润九价HPV疫苗也已处于临床研究阶段,目前正在开展Ⅲ期临床研究受试者入组前的相关准备工作。
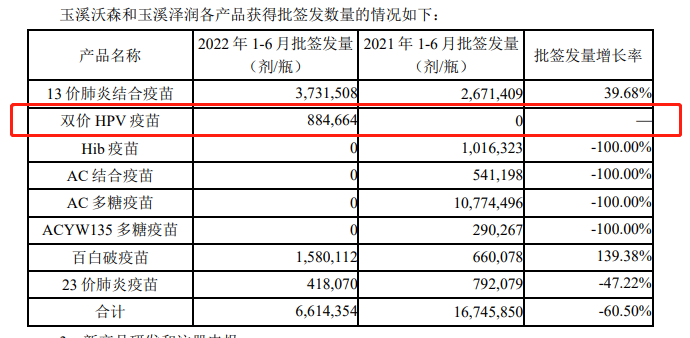
值得注意的是,今年3月,沃森生物子公司玉溪泽润二价HPV疫苗于3月获得《药品注册证书》,5月首批产品获得《生物制品批签发证明》,上半年,玉溪泽润二价HPV疫苗共获得批签发884664剂。
此外,上海博唯的九价疫苗三期临床试验仍在进行中。贝壳财经记者注意到,今年5月,广东阳春疾控还曾发布志愿者招募信息称,博唯四价人乳头瘤病毒(HPV)疫苗持久性免疫临床研究项目即将启动,申办方是上海博唯生物科技有限公司,负责机构是广东省疾病预防控制中心、广东省生物制品与药物研究所,现场设在阳春市疾病预防控制中心。
国产九价还要等多久? 康乐卫士:预计2027获批上市
我国多家企业的九价HPV疫苗研发已经进入临床三期阶段,那么距离上市还有多远?
以同样进入临床三期试验的康乐卫士为例,该公司在8月6日披露的半年度报告中介绍,公司在3月启动九价HPV疫苗小年龄组免疫桥接临床试验,目前正在进行九价HPV疫苗(女性适应症)三期临床试验,报告期内己完成受试者三剂接种工作,正在开展病例监测随访。
康乐卫士称,九价HPV疫苗女性小年龄组免疫桥接临床试验,目的为评价九价HPV疫苗在9-19周岁健康青少年女性中的安全性和免疫原性,并考察其在青少年女性中诱导的免疫应答相比20-26周岁健康成年女性中诱导的免疫应答的非劣效性,及免疫应答的持久性。
对比来看,万泰生物旗下九价HPV疫苗、瑞科生物旗下HPV疫苗分别完成小年龄桥接临床试验完成入组,以及小年龄组免疫桥接受试者入组和首剂接种工作。
完成受试者三剂接种工作后,还需要进入检测阶段。今年3月康乐卫士发布的招股说明书中提到,公司九价HPV疫苗(女性适应症)Ⅲ期临床试验后续需进行9次病例监测阶段随访,每次随访时间间隔为6个月。
“公司计划于2025年完成第6次病例监测随访后,进行Ⅲ期临床试验期中分析。公司预计于2026年底完成全部受试者随访并提交九价HPV疫苗(女性适应症)BLA申请,2027年九价HPV疫苗(女性适应症)正式获批上市。”
值得一提的是,康乐卫士九价HPV疫苗的(男性适应症)在研项目已进入Ⅰ期临床,十五价HPV疫苗已取得国家药监局的临床试验批准通知书。
“公司计划于2025年底完成第5次病例监测随访后,进行Ⅲ期临床试验期中分析,于 2027年底完成全部受试者随访并提交BLA申请,且预计2028年九价HPV疫苗(男性适应症)正式获批上市。”康乐卫士称。
(文章来源:新京报)

 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏

